固相法合成 Na–β"-Al2O3固体电解质陶瓷
王竹梅,张天峰,左洪威,谢志翔,李月明,程亮
以工业氧化铝为原料,采用低成本埋烧工艺,用传统固相法制备Na-β"-Al2O3相相对含量高的固体电解质陶瓷材料。采用综合热分析仪、X射线衍射以及扫描电子显微镜对样品进行表征,采用交流阻抗法测试了样品的电导率。结果表明:βʺ-Al2O3相的相对含量与配方Na1.67(1+x)Li0.33Al10.67O17中的Na含量和合成温度密切相关,陶瓷在x=0.15、烧结温度为1580℃时,βʺ-Al2O3相的相对含量最高,达97.19%,此时陶瓷的微观结构较致密,300℃的电导率为0.028S/cm、电导活化能为0.259eV。该方法制备工艺简单、适合工业大规模生产。
进入21世纪以来,能源问题成为了世界各国关注的焦点,钠硫电池作为一种新型的储能电池,因其具有比能量高、放电功率大、无自放电、成本低、无污染等诸多优点而成为研究热点。钠硫电池的性能取决于其固体电解质β”-Al2O3的性质,因此,β”-Al2O3电解质的制备和性能研究也逐渐成为备受重视的研究领域。
β″-Al2O3是一种复杂的钠铝复合氧化物,经验式为Na2O·5.33Al2O3,它还有另外一种同质异构物β-Al2O3,经验式为Na2O·11Al2O3。β″-Al2O3的电导率是β-Al2O3的数10倍,但在Na2O-Al2O3体系中往往同时存在β-Al2O3与β″-Al2O3两种晶相,且在高温烧结过程中,β″-Al2O3相极易向β-Al2O3相转变,因而,想要制得β″-Al2O3相含量高的固体电解质材料较为困难。
传统合成β”-Al2O3的主要方法是将高纯α-Al2O3、Na2CO3及少量稳定剂如MgO或Li2O等混合,在1580℃以上的高温下烧结而成,此法因使用高纯α-Al2O3原料使得成本较高。近十几年来,出现了一些关于采用新式化学方法如溶胶-凝胶法、醇盐水解法、溶剂燃烧法、共沉淀法法等制备β”-Al2O3的相关报道,这些合成方法具有合成材料纯度高、分布均匀、烧结温度低等优点,但其合成工艺较为繁杂、设备和操作要求较高,相对于传统固相法难以工业化大生产。另外,由于Na2O在高温烧结时极易挥发,因而无论采用传统固相法还是新式化学法制备β″-Al2O3,为了保证陶瓷烧结后的性能,往往在素坯烧结时,均需将素坯埋入预合成的前驱体中进行埋烧,这样的埋烧工艺使得生产成本大幅增加。
采用固相合成法,使用低成本的工业级α-Al2O3(纯度为82.90%,主要杂质为结晶水)为原料,同时改进埋烧工艺,将埋烧料分为两部分,一部分为少量的预合成前驱体,另一部分为大量的工业级α-Al2O3,从而降低埋烧成本,埋烧示意图见图1,探索了钠含量和烧成制度对β″-Al2O3相含量的影响,获得了性能较好的配方组成及烧成制度,该制备方法成本低,易于工业化大量生产,具有很好的应用价值。
1 实验
1.1 样品制备
采用工业级Al2O3、分析纯Na2CO3、分析纯Li2CO3为原料,按照Na1.67(1+x)Li0.33Al10.67O17(x=0,0.10,0.15,0.20)的化学计量比配料。将称好的原料置于球磨罐中,以无水乙醇和ZrO2球磨子为球磨介质球磨12h。将球磨好的浆料烘干后在1100℃预烧2h,将预烧后的粉料用研钵粗磨后置于球磨罐中二次球磨12h,烘干,过筛后加入质量分数为3%的聚乙烯酸缩丁醛(PVB)黏结剂造粒,等静压机下压制成直径为13mm、厚度为1.3mm左右的圆柱体。排胶后在不同的烧结温度下煅烧,保温30min,随炉冷却至室温。
1.2 样品表征用S-4800场发射扫描电子显微镜观察样品的形貌,工作电压3kV。用AXSD8ADVANCE型X射线衍射仪(XRD)检测样品的晶相组成,工作电压40kV,电流40mA,CuKα(λ=0.15418nm),扫描角5°~70°。用DT-50型热分析仪(SHIMADZU,JAPAN)检测一次球磨后粉料的热物理性能,氦气氛,升温速率10℃/min,温度范围室温~1400℃。用交流阻抗谱测试技术在CHI604C电化学测试站上测试样品的电导率,样品抛光后两面被烧银电极,用银丝引出作为电极引线,测试温度范围250~700℃,测试频率范围为10-1~105Hz,交流输入信号为10mV。
2 结果与讨论
2.1 热物理性能分析
为了研究粉料在不同温度下所发生的热物理变化,将一次球磨后x=0.15的粉料进行了差热-热重(TG-DTA)测试,如图2所示。由图2可见,在110.8℃处有1个明显的吸热峰,同时在TG曲线上伴随着质量的剧烈损失,这可以归结为游离水和残余乙醇的挥发;在224.4℃出现了1个微小的吸热峰,同时伴随着质量的快速减少,这可能是原料中含有的少量结晶水脱水所致;在345.6℃出现了1个明显的放热峰,同时伴随着质量的减少,这可能是粉料中残留的乙醇等有机物燃烧所造成的;在740.9℃处有1个明显的吸热峰,同时伴随着质量的快速减少,这是由于粉体中Na2CO3、Li2CO3发生分解反应,分解为Na2O、Li2O并放出CO2所致;在900~1250℃区间有1个缓慢的放热峰,质量损失并不明显,这是由于α-Al2O3与Na2O、Li2O反应形成βʺ-Al2O3、β-Al2O3、NaAl5O8和LiAl5O8所致。另外,由800~1400℃区间的TG曲线可见,虽然质量损失不明显,但仍可观察到质量缓慢的匀速减小,质量损失约为1.21%,这可归结于Na2O的挥发,由于质量损失少,并未观察到吸热峰。由于TG-DTA分析具有一定的滞后性;同时,参考其他相关文献,将预烧温度设定为1100℃。
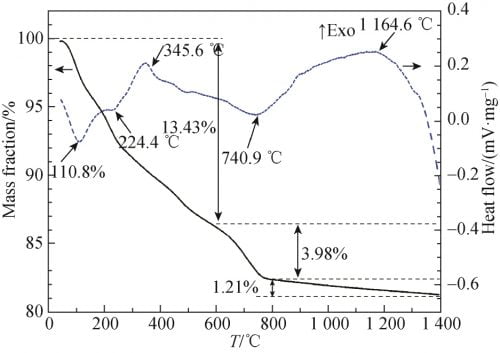
图 2 Na1.67(1+x)Li0.33Al10.67O17(x=0.15)陶瓷原料的 TG–DTA 曲线
2.2 XRD分析
图3为不同配方粉体在1100℃预烧后制得前驱体的XRD谱。从图3可以看出,所有样品均观察到βʺ-Al2O3和NaAl5O8特征峰,且均未观察到α-Al2O3和β-Al2O3相衍射峰,说明该预烧温度下,原料中的α-Al2O3几乎已经完全反应,且此时β相含量很少,不能在XRD谱观察到;同时,XRD谱中出现了3个未知峰,可能是一些复杂的Na、Al、O化合物;当x=0和x=0.1时,XRD谱中βʺ-Al2O3和NaAl5O8相所对应的衍射峰较宽、衍射峰强度较低,表明产物结晶度不高;当x值逐渐增大至0.15和0.20时,βʺ-Al2O3和NaAl5O8特征峰明显增强且尖锐,表明随着Na2O的升高,粉体预烧后结晶度提高,晶相发育更趋完善。
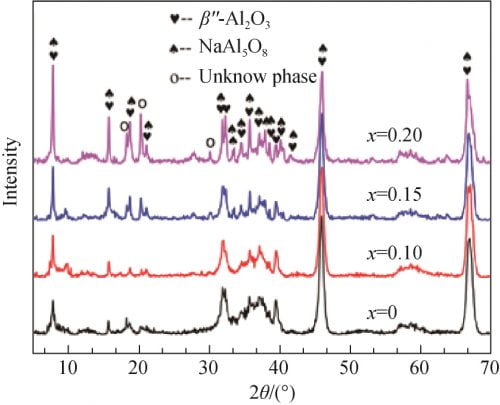
图 3 1 100 ℃预烧后各前驱体样品的 XRD 谱
图4为不同配方前驱体经压片制样后在1580℃下煅烧后的XRD谱及βʺ-Al2O3和β-Al2O3标准图谱。由图4可以看出,所有样品均为βʺ-Al2O3相和β-Al2O3相,且随着x值即Na2O含量的增加,其βʺ-Al2O3特征峰在2θ=45.9°的峰强呈先增大后减小的趋势。分别选取2θ=44.5°(β-Al2O3)和2θ=45.9°(βʺ-Al2O3)特征峰,根据式(1)[12]可计算出βʺ-Al2O3相的相对含量,结果如表1所示。由表1可见,βʺ-Al2O3相的相对含量随着配方中Na2O含量的提高呈先增加后减少的趋势,x=0.15时最大,达97.19%;当Na2O含量稍提高至x=0.20时,βʺ-Al2O3相的相对含量急剧降低至75.66%,此时可观察到明显的β-Al2O3相衍射峰(见图4,x=0.20,2θ=44.5°),这可能是由于Na2O含量过高,导致预烧时生成过多的NaAl5O8,而在烧结时没有足够的LiAl5O8与之反应生成βʺ-Al2O3相,从而生成了更多的β-Al2O3相。

其中:Iβ、Iβʺ分别为β-Al2O3与βʺ-Al2O3的特征峰强度。
表 1 不同配方样品在 1 580℃煅烧后 βʺ-Al2O3相的相对含量

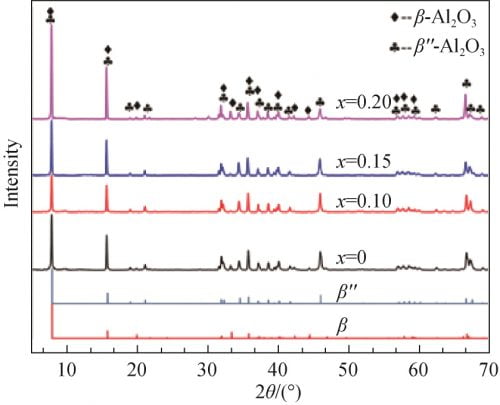
图 4 各样品在 1 580 ℃煅烧后的 XRD 谱
图5为x=0.15样品分别在1560、1580、1600℃煅烧后的XRD谱。采用式(1)相同的方法计算βʺ-Al2O3相的相对含量,如表2所示。由图5特征峰放大对比图结合表2可以看出,在1560℃烧结时,样品βʺ-Al2O3相所对应的特征衍射峰的强度较低且半峰宽较宽,说明结晶度不高,但βʺ-Al2O3相的相对含量较高,为92.02%;在1580℃时,衍射峰的强度最高且尖锐,说明该温度下晶体的结晶度最好,βʺ-Al2O3相的含量也最高,为97.19%;而在1600℃时,出现了明显的β-Al2O3相特征峰(2θ=44.5°),βʺ-Al2O3相的相对含量也下降到了66.09%。这可能是2个方面的原因造成的,一是随着温度的进一步增高,βʺ-Al2O3相向β-Al2O3相转变;二是随着温度的升高,Na2O挥发加剧,导致样品向Na含量更少的β-Al2O3相转变。
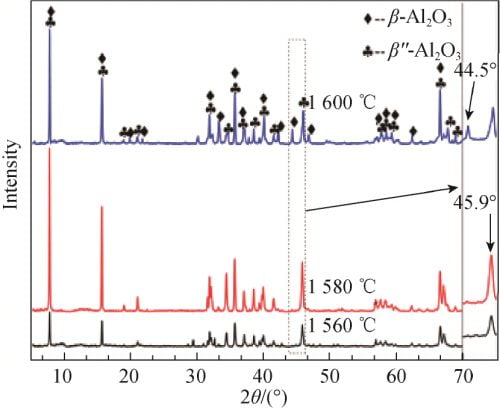
图 5 不同温度煅烧后 Na1.67(1+x)Li0.33Al10.67O17(x=0.15)陶瓷的 XRD 谱
2.3 微观形貌分析

图 6 不同温度烧结后 Na1.67(1+x)Li0.33Al10.67O17(x=0.15)陶瓷断面的 SEM 照片
图6为x=0.15样品在不同温度煅烧后的SEM照片。从图6a可以看出,样品在1560℃煅烧后仍有少量气孔,且可观察到大量的熔融态物质,结合图4可知此时样品结晶度较低;从图6b可以看出,样品在1580℃煅烧后,样品表面的晶粒尺寸较小,晶粒间有微小的尺寸差距,晶界也较为明显。从图6c可以看出,1600℃时,几乎已经观察不到晶界的存在,晶体最致密,但结合图5和表2可知,此温度下βʺ-Al2O3相的相对含量反而最低,这非常不利于Na+的传导。
表 2 x=0.15 配方不同烧结温度 βʺ-Al2O3相的相对含量

2.4 电导率分析
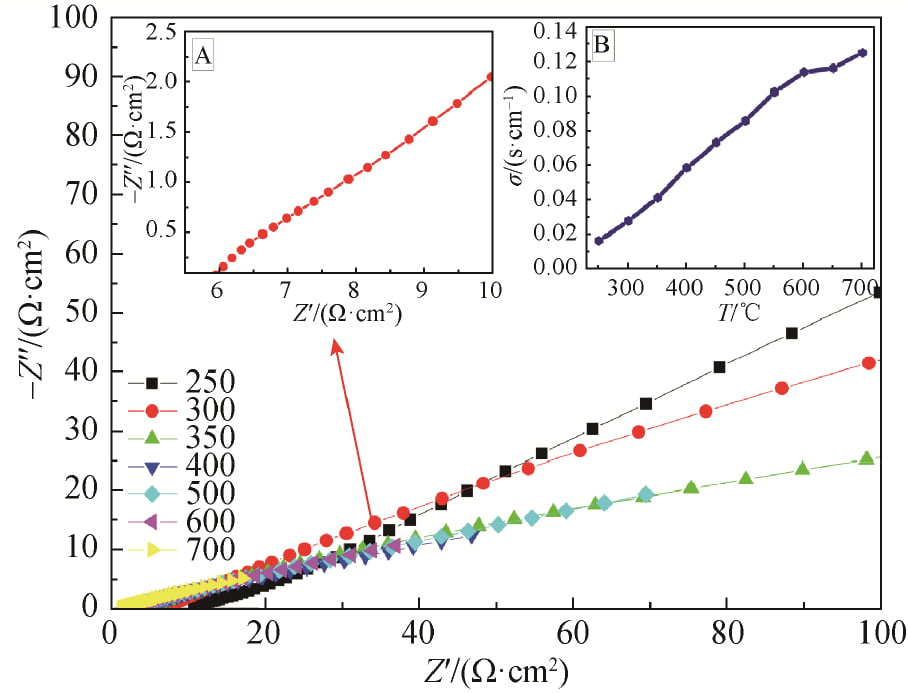
用交流阻抗仪测试了1580℃烧结后、x=0.15样品在不同温度下的交流阻抗图谱如图7所示;其中300℃的交流阻抗谱如图7中的插图A所示,求得不同温度下的电导率如图7插图B所示。由图7可以看出,随着温度的升高样品的电导率逐渐提高,样品在300℃的电导率为0.028S/cm。
2.5导电机制分析
由Arrnhenius理论导出电导率与温度相互关系[14]结果如式(2)所示。式中:A为特征常数;R为摩尔气体常数;Ea为电导活化能,包括缺陷形成能和离子迁移能。将式(2)两边取对数得式(3),将不同温度下的电导率代入式(3),得到样品的电导率和温度关系曲线如图8所示。从图8可以看出,曲线几乎为线性,由此求出晶体的电导活化能为Ea=0.259eV。
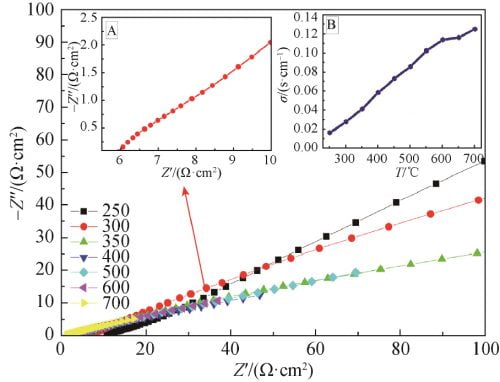
图 7 Na1.67(1+x)Li0.33Al10.67O17(x=0.15)陶瓷在 250~700 ℃的交流阻抗谱


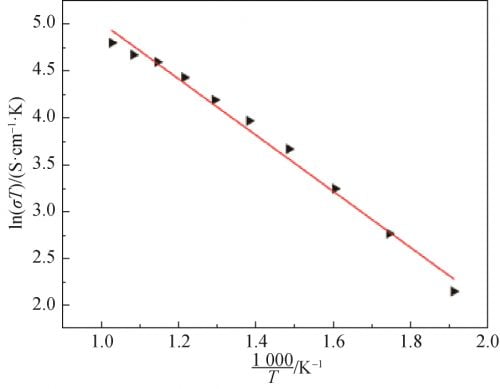
图 8 Na1.67(1+x)Li0.33Al10.67O17(x=0.15)陶瓷电导率和温度关系曲线
根据样品在300℃测量的交流阻抗谱线(Measuredvalue),参考Zhu等的研究成果[15],绘制等效电路模型如图9中插图所示,用zsimdemo软件进行拟合,得到拟合谱线(Fittedvalue)见图9,对比2条谱线可见,2条线几乎重叠,说明等效电路模型与实际电路相近。等效电路模型中,L1(Inductanceduetosilverwireandsilverelectrode)和R0(Leadwireresistance)分别为银丝和银涂层的电感和电阻;CPEg(graincapacitance)和Rg(grainresistance)分别为晶粒的电容和电阻;CPEgb(grainboundarycapacitance)和Rgb(grainboundaryresistance)分别为晶界的电容和电阻;CPEdl(adoublelayercapacitance)为双层结构电容;Rct(chargetransitionresistance)为电荷转移电阻,由于多晶陶瓷电解质的性质,纯电容在这里被一个角向量元件(CPE)所取代。
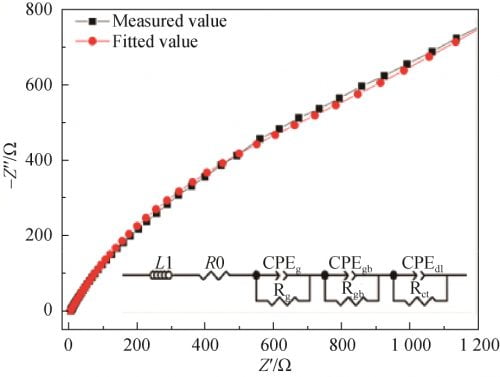
图 9 Na1.67(1+x)Li0.33Al10.67O17(x=0.15)陶瓷在 300 ℃下的拟合电路交流阻抗谱
3 结论
1)1100℃预烧已形成部分βʺ-Al2O3,且配方Na1.67(1+x)Li0.33Al10.67O17中的Na含量越高,βʺ-Al2O3相的晶相发育越完善。
2)βʺ-Al2O3相的相对含量与配方Na1.67(1+x)Li0.33Al10.67O17中的Na含量和合成温度密切相关,陶瓷在x=0.15、烧结温度为1580℃时,βʺ-Al2O3相的相对含量最高,达97.19%,此时陶瓷的微观结构较致密,300℃下的电导率为0.028S/cm、电导活化能为0.259eV。